鄰位交叉效應


在有機化學中,鄰位交叉(英語:Gauche)指的是在兩相鄰基團的二面角為60°下產生的構象異構。國際純粹與應用化學聯合會(IUPAC)定義鄰位交叉的基團需傾斜對齊連接相鄰原子的基團(傾斜對齊即:經旋轉後可以對齊)。[1]
在立體化學中,鄰位交叉的相互作用會阻礙化學鍵的轉動。以丁烷為例,它有兩種可能的交錯式構象(穩定平衡狀態),對應不同的勢能,兩個甲基可能呈反式(英語:Anti)構象,或者彼此間二面角為60°。後者兩甲基即為鄰位交叉,並且甲基間鄰位交叉相互作用產生的相對勢能為3.8KJ/mol。一般來說鄰位交叉的旋轉異構物較反式的旋轉異構物來得不穩定。
鄰位交叉效應[編輯]
在一些特定的化合物中,可能出現鄰位交叉的旋轉異構物較反式的旋轉異構物更為穩定的反常情況。這一現象被稱為鄰位交叉效應。[2] 例如:1,2-二氟乙烷(H2FCCFH2)受鄰位交叉效應影響,鄰位交叉的旋轉異構物較反式的旋轉異構物來得穩定。在氣態下,前者勢能大約比後者低2.4-3.4 KJ/mol。另一個例子是1,2-二甲氧基乙烷。
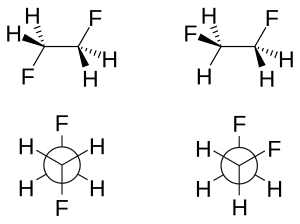

在超共軛效應模型中,認為穩定鄰位交叉異構物的原因是C-H的σ成鍵軌道提供電子密度給C-F的σ*反鍵軌道。由於氟的電負性較大,因此C-H的σ軌域是比C-F的σ軌域更好的電子供體,而C-F的σ*軌域是比C-H的σ*軌道更好的電子受體。只有鄰位交叉構型才能允許較好的供體與受體有好的重疊。
在彎曲鍵模型中,二氟乙烷的鄰位交叉效應是由於氟的電負性大,增加了兩個C-F上p軌域的性質,導致中央C-C鍵結上下左右面的電子密度增加,如果為鄰位交叉構型則結果所產生的軌域重疊減少可由彎曲鍵的形成進行部分補償。以這兩種模式來說,二氟乙烷的鄰位交叉效應的主要原因通常認為是超共軛效應。[3][4]
兩種旋轉異構物的分子結構可以經由高解像度的紅外光譜加上電腦的處理而得。[2] 根據上述的模型,反式旋轉異構物C-C鍵的鍵長比較長(154.1 pm,鄰位交叉旋轉異構物為150 pm),由於鄰位交叉旋轉異構物氟原子間立體空間上的斥力,增加了C-C-F的鍵角(3.2°),也增加F-C-C-F的二面角(從理論上的60°變成71°)。
對1,2-二氟-1,2-二苯基乙烷(相當於1,2-二氟乙烷中兩個氫被苯基取代的產物)的X射線繞射研究和質子耦合常數的測定表明,在(1R,2S)-1,2-二氟-1,2-二苯基乙烷及其對映體中,兩個苯基採取反式構象而兩個氟原子採取鄰位交叉構象。而在(1R,2R)-1,2-二氟-1,2-二苯基乙烷中,苯基和氟原子均採取鄰位交叉構象。[5]根據計算結果,這一構象比反式構象穩定0.88KJ/mol。
有文獻報道了在一個全順式四氟代的分子中觀察到了鄰位交叉效應。該分子中最後一個氟原子由以下反應引入:[6]

此外由於反式和鄰位交叉異構物的極性相差很大,因此鄰位交叉效應受溶劑效應的影響也很大。例如:2,3-二硝基-2,3-二甲基丁烷,其固態只存在鄰位交叉異構物,而其在苯溶液中鄰位交叉異構物佔79%,但四氯化碳溶液中鄰位交叉異構物佔42%。[7]
相關連結[編輯]
參考[編輯]
- ^ 國際純化學和應用化學聯合會,化學術語概略,第二版。(金皮書)(1997)。在線校正版: (2006–) "gauche"。doi:10.1351/goldbook.G02593
- ^ 2.0 2.1 Contribution to the Study of the Gauche Effect. The Complete Structure of the Anti Rotamer of 1,2-Difluoroethane Norman C. Craig, Anthony Chen, Ki Hwan Suh, Stefan Klee, Georg C. Mellau, Brenda P. Winnewisser, and Manfred Winnewisser J. Am. Chem. Soc.; 1997; 119(20) pp 4789 - 4790; (Communication) doi:10.1021/ja963819e
- ^ Goodman, L.; Gu, H.; Pophristic, V.. Gauche Effect in 1,2-Difluoroethane. Hyperconjugation, Bent Bonds, Steric Repulsion. J. Phys. Chem. A. 2005, 109, 1223-1229. doi:10.1021/jp046290d
- ^ David O'Hagan. Understanding organofluorine chemistry. An introduction to the C–F bond. Chem. Soc. Rev. 2008 doi:10.1039/b711844a
- ^ The vicinal difluoro motif: The synthesis and conformation of erythro- and threo- diastereoisomers of 1,2-difluorodiphenylethanes, 2,3-difluorosuccinic acids and their derivatives O'Hagan D, Rzepa H, Schuler M, Slawin A Beilstein Journal of Organic Chemistry, 2006 2:19 ( 2 October 2006 ) doi:10.1186/1860-5397-2-19
- ^ Enantioselective Synthesis of an All-syn Four Vicinal Fluorine Motif Luke Hunter, David O'Hagan, and Alexandra M. Z. Slawin J. Am. Chem. Soc.; 2006; 128(51) pp 16422 - 16423; (Communication) doi:10.1021/ja066188p
- ^ Smith, Michael. B.; March, J. March's Advanced Organic Chemistry, 7th edition. Wiley, 2001.p177-178 ISBN 978-0-470-46259-1
